Alcheimera slimība, kas ir visizplatītākais gados vecāku cilvēku gadījums, ir skārusi lielāko daļu cilvēku.
Viens no izaicinājumiem Alcheimera slimības ārstēšanā ir tas, ka terapeitisko zāļu piegādi smadzeņu audiem ierobežo hematoencefāliskā barjera. Pētījumā atklājās, ka MRI vadīta zemas intensitātes fokusēta ultraskaņa var atgriezeniski atvērt hematoencefālisko barjeru pacientiem ar Alcheimera slimību vai citiem neiroloģiskiem traucējumiem, tostarp Parkinsona slimību, smadzeņu audzējiem un amiotrofisko laterālo sklerozi.
Nesen Rietumvirdžīnijas Universitātes Rokfellera Neiroloģijas institūtā veikts neliels koncepcijas pierādījuma pētījums parādīja, ka pacientiem ar Alcheimera slimību, kuri saņēma adukanumaba infūziju kombinācijā ar fokusētu ultraskaņu, īslaicīgi atvērās hematoencefāliskā barjera, kas ievērojami samazināja smadzeņu amiloīda beta (Aβ) slodzi pētījuma pusē. Pētījums varētu pavērt jaunas durvis smadzeņu slimību ārstēšanai.
Hematoencefāliskā barjera aizsargā smadzenes no kaitīgām vielām, vienlaikus ļaujot iekļūt svarīgām uzturvielām. Taču hematoencefāliskā barjera arī novērš terapeitisko zāļu piegādi smadzenēm, kas ir īpaši aktuāla problēma Alcheimera slimības ārstēšanā. Pasaulei novecojot, Alcheimera slimības slimnieku skaits gadu no gada pieaug, un tās ārstēšanas iespējas ir ierobežotas, radot lielu slogu veselības aprūpei. Adukanumabs ir amiloīda beta (Aβ) saistoša monoklonāla antiviela, ko ASV Pārtikas un zāļu pārvalde (FDA) ir apstiprinājusi Alcheimera slimības ārstēšanai, taču tās iekļūšana hematoencefāliskā barjerā ir ierobežota.
Fokusēta ultraskaņa rada mehāniskus viļņus, kas izraisa svārstības starp saspiešanu un atšķaidīšanu. Kad burbuļi tiek ievadīti asinīs un pakļauti ultraskaņas laukam, tie saspiežas un izplešas vairāk nekā apkārtējie audi un asinis. Šīs svārstības rada mehānisku spriegumu uz asinsvadu sieniņas, izraisot ciešo savienojumu starp endotēlija šūnām stiepšanos un atvēršanos (attēls zemāk). Tā rezultātā tiek apdraudēta hematoencefāliskā barjera integritāte, ļaujot molekulām difundēt smadzenēs. Hematoencefāliskā barjera sadzīst pati no sevis aptuveni sešu stundu laikā.
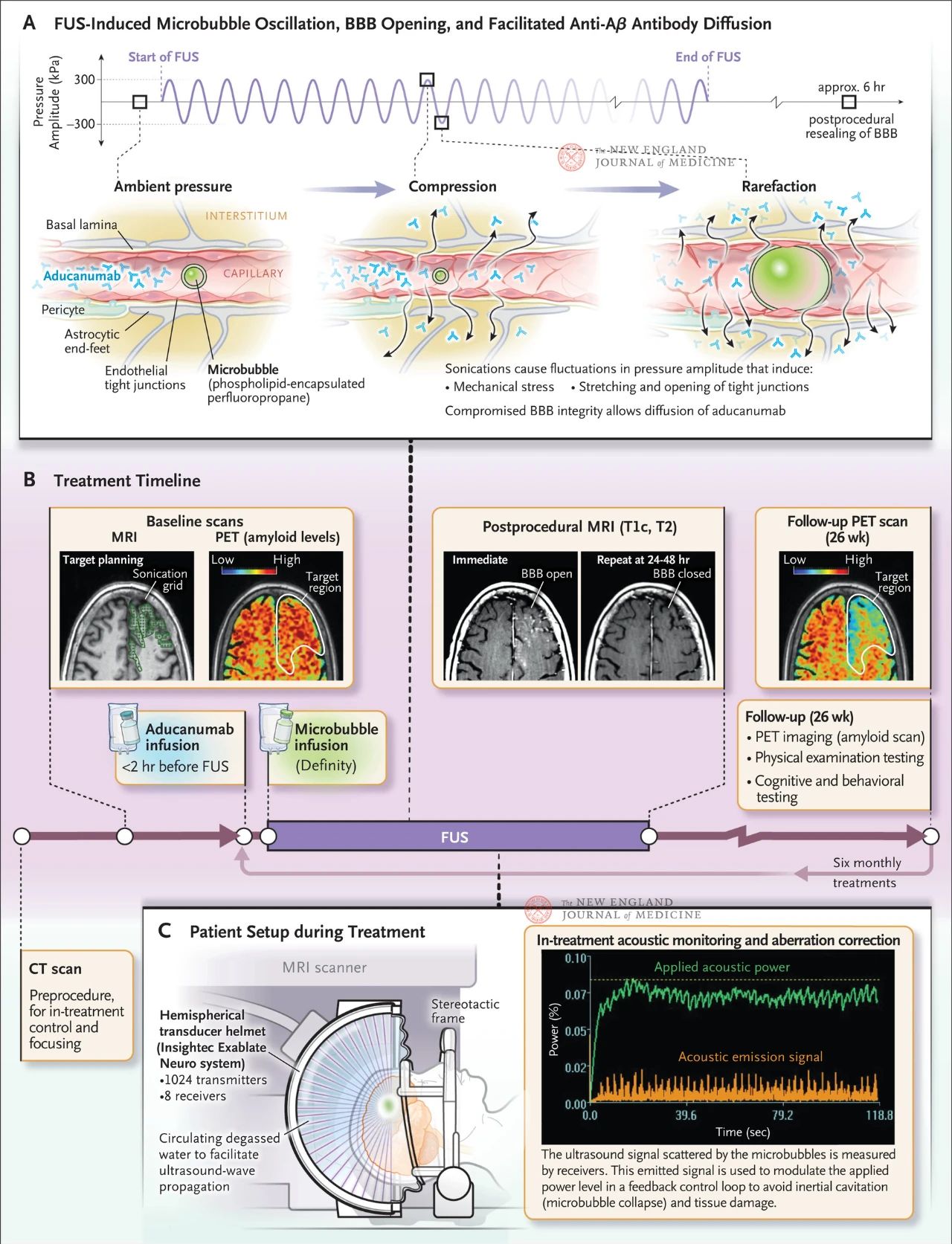
Attēlā parādīta virziena ultraskaņas ietekme uz kapilāru sieniņām, kad asinsvados ir mikrometra izmēra burbuļi. Gāzes augstās saspiežamības dēļ burbuļi saraujas un izplešas vairāk nekā apkārtējie audi, radot mehānisku stresu endotēlija šūnām. Šis process izraisa ciešu savienojumu atvēršanos un var arī izraisīt astrocītu galu atdalīšanos no asinsvadu sieniņas, apdraudot hematoencefāliskā barjeras integritāti un veicinot antivielu difūziju. Turklāt endotēlija šūnas, kas pakļautas fokusētai ultraskaņai, pastiprināja savu aktīvo vakuolu transporta aktivitāti un nomāca izplūdes sūkņa funkciju, tādējādi samazinot smadzeņu antivielu klīrensu. B attēlā parādīts ārstēšanas grafiks, kas ietver datortomogrāfiju (DT) un magnētiskās rezonanses attēlveidošanu (MRI), lai izstrādātu ultraskaņas ārstēšanas plānu, 18F-flubitabāna pozitronu emisijas tomogrāfiju (PET) sākotnējā stāvoklī, antivielu infūziju pirms fokusētas ultraskaņas terapijas un mikrovezikulāru infūziju ārstēšanas laikā, kā arī mikrovezikulārās izkliedes ultraskaņas signālu akustisko uzraudzību, ko izmanto ārstēšanas kontrolei. Pēc fokusētas ultraskaņas terapijas iegūtie attēli ietvēra T1 svērto kontrasta pastiprinātu MRI, kas parādīja, ka hematoencefāliskā barjera bija atvērta ultraskaņas apstrādātajā zonā. Pēc 24 līdz 48 stundu ilgas fokusētas ultraskaņas terapijas tajā pašā apgabalā tika novērota pilnīga hematoencefāliskā barjeras sadzīšana. Vienam no pacientiem 26 nedēļas vēlāk veiktā 18F-flubitabāna PET skenēšana novērošanas laikā uzrādīja samazinātu Aβ līmeni smadzenēs pēc ārstēšanas. C attēlā parādīta MRI vadīta fokusētas ultraskaņas iekārta ārstēšanas laikā. Puslodes formas pārveidotāja ķivere satur vairāk nekā 1000 ultraskaņas avotu, kas, izmantojot MRI reāllaika vadību, saplūst vienā fokusa punktā smadzenēs.
2001. gadā pirmo reizi tika pierādīts, ka fokusēta ultraskaņa pētījumos ar dzīvniekiem izraisa hematoencefāliskā barjeras atvēršanos, un turpmākie preklīniskie pētījumi ir parādījuši, ka fokusēta ultraskaņa var uzlabot zāļu piegādi un efektivitāti. Kopš tā laika ir atklāts, ka fokusēta ultraskaņa var droši atvērt hematoencefālisko barjeru pacientiem ar Alcheimera slimību, kuri nesaņem medikamentus, un var arī piegādāt antivielas pret krūts vēža metastāzēm smadzenēs.
Mikroburbuļu piegādes process
Mikroburbuļi ir ultraskaņas kontrastviela, ko parasti izmanto asins plūsmas un asinsvadu novērošanai ultraskaņas diagnostikā. Ultraskaņas terapijas laikā intravenozi tika ievadīta ar fosfolipīdiem pārklāta nepirogēna oktafluorpropāna burbuļu suspensija (1.B attēls). Mikroburbuļi ir ļoti polidispersi, to diametrs svārstās no mazāk nekā 1 μm līdz vairāk nekā 10 μm. Oktafluorpropāns ir stabila gāze, kas netiek metabolizēta un var tikt izvadīta caur plaušām. Lipīdu apvalks, kas aptver un stabilizē burbuļus, sastāv no trim dabīgiem cilvēka lipīdiem, kas tiek metabolizēti līdzīgi kā endogēnie fosfolipīdi.
Fokusētas ultraskaņas ģenerēšana
Fokusētu ultraskaņu ģenerē puslodes formas pārveidotāja ķivere, kas apņem pacienta galvu (1.C attēls). Ķivere ir aprīkota ar 1024 neatkarīgi vadāmiem ultraskaņas avotiem, kas dabiski ir fokusēti puslodes centrā. Šos ultraskaņas avotus darbina sinusoidāli radiofrekvences spriegumi, un tie izstaro ultraskaņas viļņus, kurus vada magnētiskās rezonanses attēlveidošana. Pacients valkā ķiveri, un ap galvu cirkulē degazēts ūdens, lai atvieglotu ultraskaņas pārraidi. Ultraskaņa pārvietojas caur ādu un galvaskausu uz smadzeņu mērķi.
Izmaiņas galvaskausa biezumā un blīvumā ietekmēs ultraskaņas izplatīšanos, kā rezultātā ultraskaņas sasniegšanai bojājumā būs nedaudz atšķirīgs laiks. Šo kropļojumu var koriģēt, iegūstot augstas izšķirtspējas datortomogrāfijas datus, lai iegūtu informāciju par galvaskausa formu, biezumu un blīvumu. Datorsimulācijas modelis var aprēķināt katra piedziņas signāla kompensēto fāzes nobīdi, lai atjaunotu aso fokusu. Kontrolējot RF signāla fāzi, ultraskaņu var elektroniski fokusēt un pozicionēt tā, lai tā aptvertu lielu audu daudzumu, nepārvietojot ultraskaņas avota masīvu. Mērķa audu atrašanās vieta tiek noteikta, veicot galvas magnētiskās rezonanses attēlveidošanu, kamēr tai ir uzlikta ķivere. Mērķa tilpums ir aizpildīts ar trīsdimensiju ultraskaņas enkurpunktu režģi, kas katrā enkurpunktā izstaro ultraskaņas viļņus 5–10 ms, atkārtojot ik pēc 3 sekundēm. Ultraskaņas jauda tiek pakāpeniski palielināta, līdz tiek noteikts vēlamais burbuļu izkliedes signāls, un pēc tam tiek turēta 120 sekundes. Šis process tiek atkārtots ar citiem tīkliem, līdz mērķa tilpums ir pilnībā pārklāts.
Lai atvērtu hematoencefālisko barjeru, skaņas viļņu amplitūdai jāpārsniedz noteikts slieksnis, virs kura barjeras caurlaidība palielinās līdz ar spiediena amplitūdas pieaugumu, līdz rodas audu bojājumi, kas izpaužas kā eritrocītu eksosmoze, asiņošana, apoptoze un nekroze, kas visi bieži ir saistīti ar burbuļa sabrukšanu (ko sauc par inerciālo kavitāciju). Slieksnis ir atkarīgs no mikroburbuļu izmēra un apvalka materiāla. Nosakot un interpretējot mikroburbuļu izkliedētos ultraskaņas signālus, iedarbību var uzturēt drošā diapazonā.
Pēc ultraskaņas terapijas tika veikta T1 svērtā MRI ar kontrastvielu, lai noteiktu, vai mērķa vietā ir atvērta hematoencefāliskā barjera, un T2 svērtie attēli tika izmantoti, lai apstiprinātu, vai ir notikusi ekstravazācija vai asiņošana. Šie novērojumi sniedz norādījumus citu ārstēšanas metožu pielāgošanai, ja nepieciešams.
Terapeitiskās iedarbības novērtējums un perspektīva
Pētnieki kvantitatīvi novērtēja ārstēšanas ietekmi uz Aβ daudzumu smadzenēs, salīdzinot 18F-flubitabāna pozitronu emisijas tomogrāfiju pirms un pēc ārstēšanas, lai novērtētu Aβ tilpuma atšķirību starp apstrādāto zonu un līdzīgu zonu pretējā pusē. Iepriekšējie tās pašas komandas pētījumi ir parādījuši, ka vienkārša ultraskaņas fokusēšana var nedaudz samazināt Aβ līmeni. Šajā pētījumā novērotais samazinājums bija vēl lielāks nekā iepriekšējos pētījumos.
Nākotnē ārstēšanas paplašināšana uz abām smadzeņu pusēm būs kritiski svarīga, lai novērtētu tās efektivitāti slimības progresēšanas aizkavēšanā. Turklāt ir nepieciešami vairāk pētījumu, lai noteiktu ilgtermiņa drošību un efektivitāti, un plašākai pieejamībai ir jāizstrādā izmaksu ziņā efektīvas terapeitiskās ierīces, kas nav atkarīgas no tiešsaistes MRI vadības. Tomēr šie atklājumi ir radījuši optimismu, ka ārstēšana un zāles, kas iznīcina Aβ, galu galā varētu palēnināt Alcheimera slimības progresēšanu.
Publicēšanas laiks: 2024. gada 6. janvāris